Dans une étude clinique de phase 1, des scientifiques dirigés par l’EPFL et leurs partenaires ont montré qu’un nouveau médicament oral ciblant le foie et l’intestin peut faire diminuer en toute sécurité les triglycérides et d’autres lipides sanguins.
Lorsque nous mangeons, notre corps convertit les calories excédentaires, en particulier les glucides, le sucre, les graisses et l’alcool, en molécules appelées «triglycérides». Les triglycérides sont une forme de graisse ou lipide, que le corps stocke dans ses cellules adipeuses comme carburant énergétique entre les repas.
Cependant, comme on le sait, un excès de graisse dans le corps peut être dangereux, provoquant une maladie appelée «hypertriglycéridémie» (ce qui signifie excès de triglycérides dans le sang). Celle-ci augmente significativement le risque de maladie cardiaque, d’accident vasculaire cérébral et de pancréatite. C’est pourquoi il est généralement conseillé d’adopter un mode de vie sain en matière d’alimentation et d’exercice physique, tandis que les cas graves nécessitent un traitement médicamenteux.
Diminuer l’activité d’un récepteur
Maîtriser le taux de lipides dans le sang repose sur un équilibre minutieux. Le foie et l’intestin libèrent des particules de graisse dans la circulation sanguine, tandis que les enzymes les décomposent et les éliminent. Lorsque la production de graisses dépasse leur élimination, les triglycérides s’accumulent, ouvrant la voie à des maladies métaboliques, comme la dyslipidémie, la pancréatite aiguë et la stéatose hépatique associée à un dysfonctionnement métabolique (MASLD).
L’un des principaux régulateurs de ce système est une protéine appelée Liver X Receptor, ou LXR, qui contrôle plusieurs gènes impliqués dans la fabrication et la métabolisation des graisses.
Lorsque le LXR est actif, les triglycérides et le cholestérol ont tendance à augmenter. La diminution de l’activité du LXR à l’aide de médicaments semble prometteuse, mais, comme le récepteur est également impliqué dans d’autres voies protectrices du cholestérol de l’organisme, le bloquer partout pourrait faire plus de mal que de bien. Ce dilemme freine les progrès dans le domaine depuis des années.
Un médicament qui cible spécifiquement le LXR hépatique
Une équipe, dirigée par Johan Auwerx de l’EPFL et Mani Subramanian d’OrsoBio ont résolu ce problème avec un composé administré par voie orale capable de réprimer l’activité du LXR, en particulier dans le foie et l’intestin, afin de réduire les triglycérides sans perturber les voies protectrices du cholestérol dans l’organisme.
Le composé TLC‐2716 est ce qu’on appelle un «agoniste inverse» du LXR. Contrairement à un «bloqueur» (antagoniste), qui empêche simplement l’activation d’un récepteur, un «agoniste inverse» fait que le récepteur envoie un signal opposé de ce qu’il enverrait normalement.
L’étude, publiée dans Nature Medicine, est la première de ce type à avoir été réalisée sur des êtres humains.
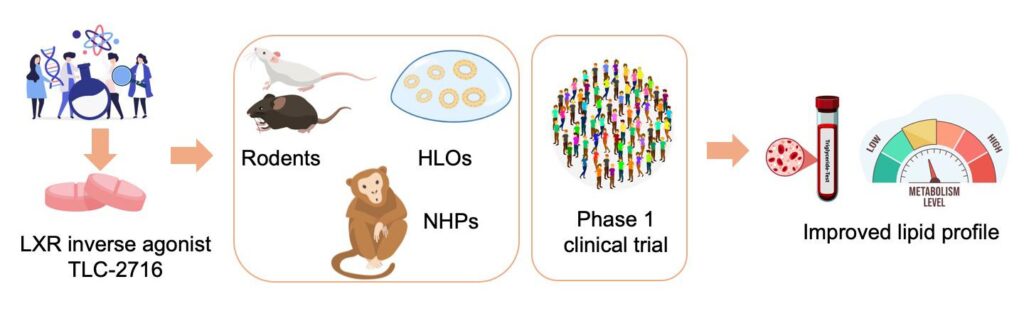
Crédit: X. Li/© 2026 EPFL
Analyse d’ensembles de données génétiques pour trouver le bon variant de récepteur
Les scientifiques ont commencé par analyser de vastes ensembles de données génétiques humaines pour déterminer quel variant de LXR est lié aux biomarqueurs des triglycérides élevés dans le sang. Les données ont mis en évidence des variants génétiques au sein du LXRα, qui est fortement exprimé dans le foie.
Cela a été attesté par la «randomisation mendélienne», une méthode génétique performante qui détermine les relations de cause à effet entre l’expression des gènes et les résultats. Dans ce cas, elle a confirmé un lien de causalité entre le gène LXRα et les troubles métaboliques: une expression plus élevée du gène LXRα peut entraîner l’augmentation des triglycérides.
Les résultats ont aidé à sélectionner le TLC‐2716 comme composé efficace pour tester le LXRα.
Test du composé
Les chercheuses et chercheurs sont ensuite passés de l’ordinateur au laboratoire. Dans les modèles de maladies métaboliques chez les rongeurs, le TLC‐2716 et un composé apparenté ont réduit les triglycérides et le cholestérol dans le sang et diminué l’accumulation de graisses dans le foie. Parallèlement, des expériences menées sur des organoïdes hépatiques humains (modèles miniatures cultivés en laboratoire de tissus hépatiques malades) ont montré la même tendance, avec moins d’accumulation de lipides et moins d’inflammation et de fibrose.
Étape suivante: la sécurité. Des études toxicologiques menées sur des souris et des primates non humains, associées à des analyses pharmacocinétiques, ont montré que le TLC‐2716 reste en grande partie dans le foie et l’intestin. Cela est essentiel, car cela limite l’exposition à d’autres tissus où l’inhibition du LXR pourrait être risquée, résolvant ainsi le problème principal du développement de médicaments pour traiter des maladies métaboliques liées à un taux élevé de triglycérides dans l’organisme.
L’essai clinique
Les résultats de laboratoire ont ouvert la voie à une étude de phase 1 randomisée et contrôlée par placebo, menée chez des adultes en bonne santé. Les participantes et participants se sont vu administrer le TLC‐2716 pendant 14 jours, à raison d’une seule dose par jour. L’essai s’est d’abord concentré sur l’innocuité et la tolérance, et les auteurs indiquent que le médicament a répondu aux critères d’évaluation principaux.
Même cet essai de courte durée a eu des effets évidents: les participantes et participants qui ont reçu des doses plus élevées de TLC‐2716 ont présenté des baisses notables des triglycérides ainsi que du cholestérol résiduel. Aux doses les plus élevées de TLC‐2716 (12 mg), les triglycérides ont diminué jusqu’à 38,5%, tandis que le cholestérol résiduel postprandial (après les repas) a chuté jusqu’à 61%. Cela s’est produit bien que les participantes et participants aient commencé avec des taux de lipides relativement normaux et n’aient pas pris d’autres médicaments hypolipémiants.
Le traitement a également accéléré l’élimination des triglycérides en réduisant l’activité de deux protéines qui la ralentissent normalement, ApoC3 et ANGPTL3. Parallèlement, l’essai n’a pas détecté de diminution de l’expression cellulaire des gènes ABCA1 et ABCG1, utilisés ici comme marqueurs liés au transport inverse du cholestérol.
Les résultats de l’essai montrent que la réduction sélective de l’activité du LXR dans le foie et l’intestin par le composé TLC‐2716 pourrait offrir une nouvelle façon, complémentaire à d’autres approches, de lutter contre les taux élevés de triglycérides et les troubles métaboliques associés. Les données de phase 1 justifient la poursuite d’essais cliniques dans le cadre d’études de phase 2, y compris chez des personnes souffrant d’hypertriglycéridémie et de MASLD. Des essais à plus grande échelle seront nécessaires, mais, pour l’instant, le concept a fait ses preuves pour une utilisation chez les êtres humains.
L’étude toxicologique sur les primates non-humains a été menée chez Medicilon (https://medicilon.com). Les animaux provenaient de Guangzhou Xiangguan Biotech Co., Ltd.
Autres contributeurs
Centre médical de l’hôpital pour enfants de Cincinnati
WM Therapeutics
Université d’Auckland
Université d’Osaka
Financement
EPFL
National Institutes of Health (NIH)
Agence japonaise pour la recherche et le développement médicaux
Première initiative mondiale des centres de recherche internationaux (WPI) du Japon
OrsoBio
Références
Xiaoxu Li, Giorgia Benegiamo, Archana Vijayakumar, Natalie Sroda, Masaki Kimura, Ryan S. Huss, Steve Weng, Eisuke Murakami, Brian J. Kirby, Giacomo V.G. von Alvensleben, Claus Kremoser, Edward J. Gane, Takanori Takebe, Robert P. Myers, G. Mani Subramanian, Johan Auwerx. An oral, liver-restricted LXR 1 inverse agonist for dyslipidemia: preclinical development and phase 1 trial. Nature Medicine 16 janvier 2026. DOI: 10.1038/s41591-025-04169-6
Auteur : Nik Papageorgiou
Source (article original) : EPFL


