Pour les greffes de peau, la xénotransplantation pourraient permettre de soigner même les patients chez qui l’on ne peut pas prélever de peau saine. National Cancer Institute/Unsplash, CC BY
Alors que plus de 10 000 personnes attendaient une greffe d’organe en France en 2023, la pénurie de dons pousse la recherche à trouver d’autres solutions. Ainsi, les xénogreffes, qui consistent à transplanter un organe d’un donneur dont l’espèce biologique est différente de celle du receveur, représentent une piste prometteuse. Le porc est considéré comme l’espèce donneuse de choix, du fait de nombreuses similarités physiologiques et morphologiques entre les organes humains et porcins.
Des avancées importantes ont notamment été réalisées récemment, avec en 2023 une greffe de rein chez un patient en état de mort cérébral, et une greffe de cœur chez un patient américain en vie mais inéligible pour une greffe humaine. Mais la xénogreffe représente aussi une piste en chirurgie reconstructive, pour fournir des greffons de peau.
Un espoir pour réparer les plaies les plus difficiles
Si pour les organes comme le foie, le rein ou le cœur, la xénogreffe permettait de pallier la pénurie de greffons, son application en chirurgie plastique présente d’autres enjeux. C’est le cas en particulier du traitement des plaies dites complexes, des plaies graves et qui ne peuvent être traitées avec des techniques simples, et ce sans agresser les tissus sains du patient. L’impact économique et social que représente aujourd’hui le traitement de ces plaies s’alourdit rapidement, en raison de l’augmentation des coûts des soins et du vieillissement de la population.
Ces plaies complexes surviennent dans des conditions très diverses : fractures de membres, retrait de cancers graves et étendus de la peau, plaies liées aux troubles vasculaires et neurologiques des patients atteints de diabète… Elles exposent parfois à l’air libre des structures dites « nobles » comme de l’os, des tendons et des vaisseaux. Dans le pire des cas, elles conduisent à l’amputation d’un membre ou à une infection généralisée dont le point de départ est la plaie, pouvant conduire au décès.
Éviter le rejet de la greffe
La seule solution pour traiter ces plaies et éviter les complications est parfois leur couverture par des tissus prélevés sur le patient lui-même, appelés lambeaux. Ces lambeaux impliquent alors le prélèvement de peau en zone saine, ce qui peut être à l’origine de conséquences néfastes importantes (réouverture de la plaie, perte d’une fonction musculaire, lésion nerveuse, douleur…). Le patient peut également manquer de zones de prélèvement de tissus sains, avec l’impossibilité de prendre du tissu adapté à la plaie à couvrir dans le cas de patients maigres, brûlés ou multiopérés. Utiliser des lambeaux tissulaires venant de porcs dans le cadre de xénogreffes serait une solution pour contourner ces problèmes.
Néanmoins, l’utilisation des xénogreffes est limitée par les barrières immunologiques interespèces. Dans la circulation sanguine humaine, des anticorps sont en effet chargés d’identifier les marqueurs non humains, appelés xénoantigènes, présents à la surface des cellules porcines. Cette réaction immunitaire est responsable d’un phénomène de rejet hyperaigu qui aboutit inexorablement à la perte du greffon en quelques minutes.
Remplacer les cellules animales par les cellules du patient
Une méthode pour éviter cette réaction immunitaire consiste à décellulariser puis à recellulariser les greffons. La décellularisation d’organes consiste à produire une matrice sans cellules (ou acellulaire), gardant la forme initiale de l’organe d’un patient ou animal donneur mais qui n’est plus constituée que du tissu conjonctif, qui structure les organes. La décellularisation permet donc d’éliminer les cellules du donneur, tout en préservant la forme et l’environnement nutritif pour les cellules, en traitant le tissu ou l’organe avec des détergents. Comme elle n’a pas de cellules, cette matrice ne provoque pas de rejet si elle est transplantée à un patient receveur.
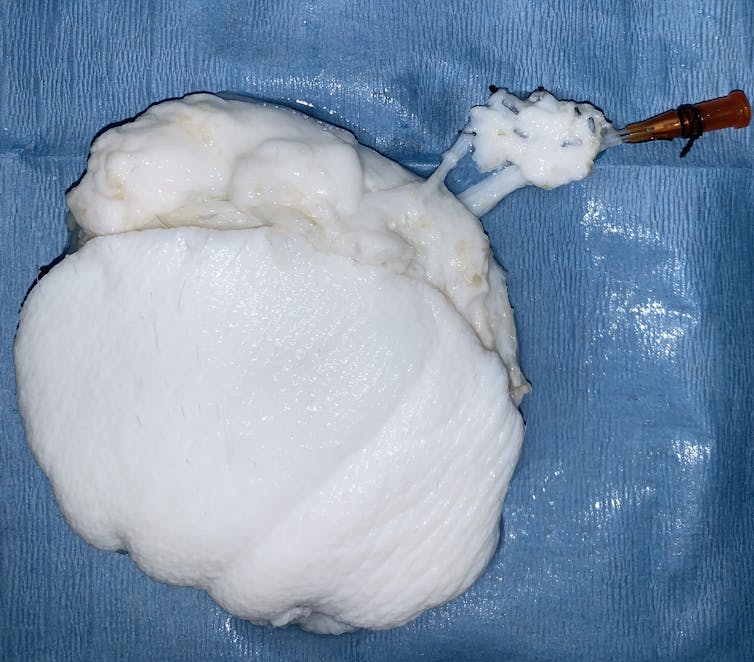
Une matrice décellularisée de peau, prélevée sur l’aine d’un porc. Elise Lupon/Université Côte d’Azur, Fourni par l’auteur
Des cellules du patient peuvent alors être cultivées sur cette matrice avant transplantation : c’est ce qu’on appelle la recellularisation. Ces matrices recellularisées peuvent être ensuite transplantées au receveur de manière à restaurer, maintenir ou améliorer la fonction de l’organe ou couvrir une plaie.
Ces matrices recellularisées sont reconnues par l’organisme du patient comme faisant partie « du soi » afin qu’il ne les rejette pas. Si un certain nombre de substituts de peau et de matrices dermiques simples et décellularisées ont été produits et commercialisés (valves cardiaques de porc, dermes artificiels bovins…), aucune greffe plus élaborée ne s’est intégrée chez un patient receveur, car les matrices requièrent dans ce cas cette étape de recellularisation.
Des avancées, mais pas encore de tentative chez l’humain
Alors que la décellularisation et la recellularisation ont montré un grand potentiel dans la transplantation d’organes comme le foie, le rein, le cœur ou le poumon, son application pour les lambeaux tissulaires n’a été étudiée que récemment. Avec mon équipe, nous avons ainsi développé et optimisé des modèles de matrices de lambeaux de peau décellularisées chez le porc. Toutes les procédures chirurgicales ont été approuvées par le comité d’éthique local.
Des lambeaux de peau ont été prélevés sur des porcs vivants et anesthésiés au bloc opératoire. Ces lambeaux ont ensuite été perfusés avec un détergent spécifique à des niveaux de concentration différents. Nous avons montré qu’il est nécessaire de garder cette concentration faible pour garder un environnement nutritif, indispensable pour accueillir de nouveau des cellules. Si la concentration de détergent est trop importante, la matrice devient toxique pour les cellules, qui ne survivent pas.
Nous avons vérifié que ces matrices de peau préservaient les propriétés mécaniques et chimiques de base de la peau porcine. Les protéines et les facteurs de croissance étaient présents en quantité suffisante dans les matrices pour que des cellules puissent y vivre. Nous avons finalement montré la possibilité de recellularisation des matrices acellulaires. Cependant, nous devons encore optimiser la stratégie de recellularisation, afin de pouvoir déposer un nombre très important de cellules sur les matrices.
Un tel traitement des greffes de lambeaux de porcs, n’induisant pas le rejet chez l’homme car contenant les cellules du patient à traiter, permettrait de s’affranchir des complications liées au prélèvement de tissu sur la peau saine du patient. Cette technologie résoudrait également les problèmes d’absence de site donneur sain. La poursuite de nos recherches est cruciale pour espérer un jour réaliser des xénotransplantation de lambeaux de peau chez l’humain sans rejet immédiat de ceux-ci.![]()
Elise Lupon, Doctorante en recherche clinique et thérapeutique, Université Côte d’Azur
Cet article est republié à partir de The Conversation sous licence Creative Commons. Lire l’article original.


